
椎旁神经阻滞对同时接受自体肋软骨移植和正颌手术的患者术后疼痛的影响:回顾性研究
引言
背景
世界各地都在进行正颌手术,以纠正下颌的解剖结构,使其恢复功能。根据具体的手术指征,如下颌不对称或下颌骨病变,可能还需要重建一个或两个颞下颌关节(temporomandibular joints,TMJ)。重建TMJ时,可以选择使用人工假体或从患者自身移植的组织[1]。尚在发育的患者通常建议使用自体移植物,特别是肋软骨移植(costochondral graft,CCG),因为这种类型的移植物包含肋骨的骨质段和软骨段,从而使得患者的下颌骨和骨骼在患者发育时可以继续生长[2-6]。然而,与不需要在其他部位手术的异体移植不同,CCG供区的疼痛不容忽视[7],目前临床上经常需要使用阿片类药物进行镇痛。
在其他围绕胸壁进行手术的外科领域,如心胸外科和乳腺外科,已采用区域麻醉技术改善手术部位的镇痛效果,包括竖脊肌平面阻滞、胸神经阻滞、前锯肌平面阻滞和胸横肌平面阻滞[8]。目前,胸壁手术中最常见的区域阻滞方法是椎旁神经阻滞(paravertebral blockade,PVB)和肋间神经阻滞(intercostal nerve blocks,INB)[8,9]。这两种方法的关键区别是,与需要在多个解剖层面进行注射的INB不同[10],PVB可以通过一次注射阻断多个节段的脊神经,从而对多个神经支配区域产生镇痛作用,有研究表明这一特性为患者提供了卓越而持久的镇痛效果[11-13]。另外,与胸段硬膜外镇痛(thoracic epidural analgesia,TEA)不同,PVB的低血压风险较低,而在低血压情况下,应用血管收缩药或者扩容等方式可能导致更坏的结果[14]。通过术前区域麻醉技术可以更好地控制术后疼痛,减少胸壁手术(如胸腔和乳房手术)术后阿片类药物的用量[10]。
理论基础和知识空白
尽管目前的证据表明,区域麻醉可以减轻胸部手术部位的疼痛,但在头颈部主要手术中应用区域麻醉的研究却很少。《整形与重建外科》杂志中有研究[7]描述了在创面缝合前将可以输注布比卡因的导管置于移植肋软骨供区,以减少术后48小时疼痛。然而,这项研究并没有进行PVB,也没有评估区域麻醉对阿片类药物用量的影响。同样,也缺乏有关在CCG正颌外科手术中应用区域镇痛或PVB的文献。
目标
鉴于以上原因,本研究的主要目标是证实这一假设:术前PVB可以更好地控制正颌手术后CCG供区的疼痛,从而减少术后阿片类药物的用量。本研究还旨在评估PVB对术后疼痛评分和住院时间(length of stay,LOS)的影响。本文内容根据STROBE报告清单条目撰写(可在https://joma.amegroups.com/article/view/10.21037/joma-22-23/rc查看)。
方法
本研究遵照《世界医学协会赫尔辛基宣言》(2013年修订),获麻省总医院机构委员会批准(编号:#2020P002222),免除个人知情同意书的签署。
研究设计
为了实现研究目的,将本研究设计为一个单中心、回顾性的队列病历回顾,在一家大型的城市教学医院进行,该医院设有口腔颌面外科(oral and maxillofacial surgery,OMFS)和麻醉住院医生项目。位于美国马萨诸塞州波士顿的麻省总医院的机构审查委员会(方案编号:2020P002222)批准了本研究的知情同意豁免权。
研究样本
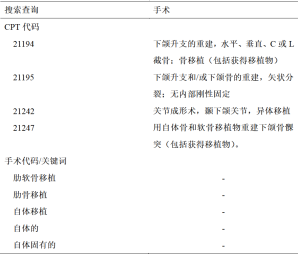
本研究纳入了在2016年1月1日—2020年12月31日期间,接受了正颌手术并同时接受单侧自体CCG进行下颌骨髁突重建的16岁及以上的所有患者。所有的正颌手术和CCG手术都是由患者所在医院的同一部门的口腔颌面外科医生进行的。通过使用结构化查询语言(structured query language,SQL),根据各种手术显示名称和当前程序术语(current procedural terminology,CPT)代码查询电子病历,确定符合条件的患者。手术名称也被用来识别潜在的病例,其中包括“肋软骨移植”“肋骨移植”“自体移植”“自体的”和“自体固有的”。用来识别潜在病例的CPT代码包括[21194][21195][21242]和[21247]。本研究的纳入标准如下:手术涉及切除一侧或两侧下颌骨髁突,并用自体肋软骨移植物重建的正颌手术。排除年龄小于16岁的患者,以防止受试者因年龄太小而无法持续报告数字疼痛评分。经回顾,将接受术前PVB的患者确定为暴露组,未接受术前PVB的患者为对照组。
术前在超声引导下进行PVB,区域麻醉小组由一名麻醉住院医生和一名麻醉主治医生组成,操作过程中进行轻度镇静。每次进行PVB时,将患者置于俯卧位,使用超声在冠状面观察由横突、胸膜和肋间膜组成的椎旁空间。然后通过平面内入路,穿刺针从外侧向内侧进针。通过水分离和直接观察确认针头是否到达椎旁空间。回抽无血后,以3 mL的等分量逐次增加、注射局部麻醉药,共约20 mL。局部麻醉药在注射部位上下1~2节段扩散,可以通过超声观察到。这个过程中可以看到胸膜的凹陷,主要由负责监督的麻醉医生进行观察并确认。此时,部分患者会进行放置PVB导管,将导管沿针头推进,然后抽出针头,固定导管,并用生理盐水在超声屏幕上观察、确认导管的位置。本研究的机构方案表明,在患者被送回手术室之前,可以通过超声观察麻醉液在适当的位置和平面上的扩散,以及冷测试(即使用酒精棉球)来确认每个区域阻滞的位置。通常不做针刺试验,但也经常有患者报告称主观感受到胸侧和背侧的皮肤节段有麻木感。
研究结果、暴露和混杂因素
人口统计学信息包括患者年龄、性别、种族、美国麻醉学会(American Society of Anesthesiology,ASA)体质状况分级、身高、体重和身体质量指数(body mass index,BMI)。主要研究结果是在达到围手术期麻醉恢复室(perioperative anesthesia care unit,PACU)转出标准之前,在PACU中应用的阿片类药物剂量,即吗啡当量剂量(morphine equivalent dose,MED)的中位数。次要研究结果是术后24小时和48小时的阿片类药物用量(MED)、患者自主报告的0~10疼痛数字评分表(numerical rating scale,NRS;即0为无痛,10为最痛)的疼痛评分,以及术后与总住院时间。PACU、重症监护室(intensive care unit,ICU)和病房的护理人员需按照NRS评分进行疼痛评估,并对患者进行疼痛药物管理,疼痛评分为1~3分(即轻度疼痛)的患者,给予泰诺和非甾体抗炎药(non-steroidal anti-inflammatory medications,NSAIDs),如布洛芬或酮咯酸;报告4~6分(即中度疼痛)的患者,给予口服阿片类药物,如羟考酮;报告7~10分(即重度疼痛)的患者,给予较强的阿片类药物,如口服和静脉注射吗啡或氢吗啡酮。所有给予患者阿片类药物的情况均从医疗记录中提取,并转换为MED进行比较。随后对所有收集到的数据进行审查,并将其制成表格。
功效和统计分析
本研究并未预先进行功效分析以指导样本量大小的确定,而是利用Epic Systems公司的电子健康记录(electronic health record,EHR)中所有可用的合格病例进行分析。虽然一般不建议进行事后功效分析,但我们收集的研究样本(N=19)产生的研究功效为0.8,在利用两个独立样本T检验比较两个研究组之间的MED时,假设集合标准差(standard deviation,SD)为3,α=0.05,可检测到最小效应值,即平均差异为2.8。这一可检测的效应值较大,由于样本量有限,本研究可能功效不足。在描述性统计中,连续变量根据数据分布情况,使用均数和SDs,或者中位数和第25/75个百分位数或标准均数差(standardized mean differences,SMD)进行报告;分类变量则使用频率和百分比进行报告。对主要和次要结果进行两个独立样本T检验或同等的非参数检验(如Wilcox检验等)来比较PVB组和非PVB组。进行Chi-square检验或Fisher精确检验。统计学意义依据相应的效应值大小(如自举中位数差异等)和95% CI及P值报告。将α值设定为0.05,对多重性不进行事后修正。所有分析均使用RStudio V2022.02(RStudio PBC,Boston, MA, USA)进行。
结果
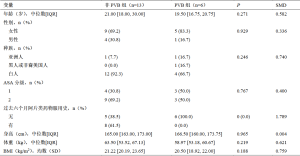
使用CPT代码和手术代码,共确定了22例符合条件的患者(见表1和图1)。排除3例年龄小于16岁的患者,最后剩下19例患者,其中6例患者接受术前PVB,13例患者未接受术前PVB(表2)。
Full table
Full table
各组患者的人口统计资料见表2。两组患者之间的年龄、性别、种族、ASA分级、身高、体重和BMI数据均没有统计学上的显著差异(表2)。非PVB组的年龄中位数比PVB组略高(21.00岁 vs 19.50岁)。参加研究的患者以女性为主,非PVB组中女性占69.2%,PVB组中占83.3%。当比较两组的种族差异时,白人最多(12 vs. 4),其次是亚洲人(1 vs. 1),然后是黑人或非裔美国人(0 vs. 1)。所有患者均为ASA 1级或2级。手术前6个月的阿片类药物使用情况有统计学意义,61.5%的非PVB组患者使用过阿片类药物,而PVB组患者无使用阿片类药物的记录,这一差异具有统计学意义,P值为0.043。最后,组间的BMI中位数没有统计学差异,非PVB组和PVB组的数值分别为21.22和20.50。
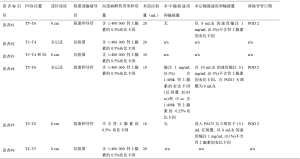
在接受PVB的6例患者中,3例患者为单次阻滞,3例患者为单次阻滞后放置导管,这些导管都在术后第2天之前被移除(表3)。有记录表明,5例PVB组患者和13例非PVB组患者接受外科医生在CCG供体内部和周围注射含1:200 000肾上腺素的0.5%利多卡因溶液,但确切的注射量并未记录。PVB组中有1例患者无手术团队在供区进行局部麻醉注射的记录。此外,外科医生还在所有患者的上颌骨、下颌骨和下颏(如果进行了颏成形术)周围的组织注射了剂量不明的含1:200 000肾上腺素的0.5%利多卡因溶液。
Full table
表4列出了不同的术前诊断、实施的手术操作和获取的肋骨的特点。两组的手术时间中位数分别为:非PVB组596.0分钟,PVB组454.5分钟,产生的中位数差异为141.5,无统计学意义,95%CI为-92—223。由于一些患者术后在ICU中仍然保留气管插管,以便观察气道,因此也测量了各组的插管时间中位数,非PVB组和PVB组的数值分别为596.0分钟和499.0分钟。这导致中位数的差异为97,95%CI为-508—220,考虑到这一范围包括0,因此也没有统计学意义。非PVB组患者的诊断中,最值得注意的是5例幼年特发性关节炎患者和3例退行性关节炎患者,而PVB组有2例幼年特发性关节炎患者和1例退行性关节炎患者。这些关节炎是炎症性的,可能与一些患者的慢性疼痛有关。各组的平均手术次数也相似,非PVB组每人4.00次,PVB组每人4.83次。所有患者均从右前侧第5或第6根肋骨处切除了1或2根肋骨,每组切除的肋骨数量相似(非PVB组为1.85根/患者,而PVB组为2.00根/患者)。各实验组获取肋骨的平均长度基本相同(分别为6.78 cm和6.67 cm)。
Full table
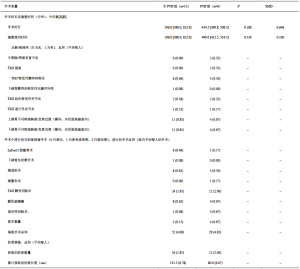
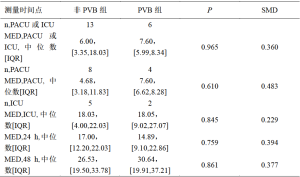
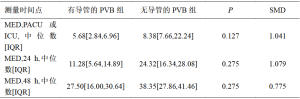
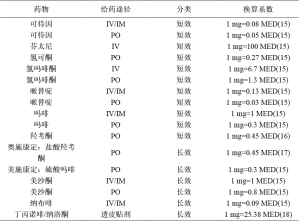
表5、表6描述了每组患者在PACU或ICU以及术后24小时和48小时内为控制疼痛而使用麻醉药的情况。用于确定每例患者的MED总量的阿片类药物换算表请见表7。比较非PVB组和PVB组,PACU/ICU期间(6.00:7.60,95%CI:-16.24—11.72)、术后24小时(17.00:14.89,95%CI:-12.11—13.76)和术后48小时(26.53:30.64,95%CI:-17.28—17.78)的MED需求中位数均没有统计学差异。只比较术后进入PACU的患者,非PVB组和PVB组的MED中位数分别为4.68和7.60(P=0.610),同样没有统计学上的显著差异。同样,只比较非PVB组和PVB组术后进入ICU的患者,MED中位数为18.03与18.05(P=0.845),也没有统计学差异。在6例接受PVB的患者中,3例只进行了单次阻滞,另外3例患者在接受阻滞后还放置了导管,但有导管的PVB组和无导管的PVB组在PACU/ICU的MED中位数(5.68 vs 8.38,P=0.127)、术后24小时的MED中位数(11.28 vs 24.32,P=0.275)或术后48小时的MED中位数(27.50 vs 38.35,P=0.275)均没有统计学差异。值得注意的是,每组中都有1例患者在术后第1天回病房前在PACU停留一晚。同样,每组中都有1例患者在ICU中保留气管插管到术后第1天,因此无法向护理人员报告自身疼痛评分,也无法在这段时间内要求使用止痛药。
Full table
Full table
Full table
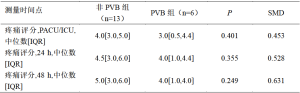
使用NRS评估和报告患者的疼痛程度,0分表示完全不痛,10分表示最痛(表8)。比较非PVB组和PVB组,疼痛评分的中位数一直较高,但在PACU/ICU(4.0 vs 3.0,95%CI:-1—5)、术后24小时(4.5 vs 4.0,95%CI:-1.68—5.00)和术后48小时(5.0 vs 4.0,95%CI:-1.98—5.49)没有统计学上的显著差异。
Full table
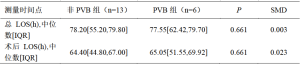
最后,表9描述了患者从到达医院到出院,以及从离开手术室到出院的LOS中位数。非PVB组与PVB组相比,总的LOS中位数没有统计学意义(78.20 vs 77.55,95%CI:-24.7—21.9),术后LOS也没有统计学意义(64.40 vs 65.05,95%CI:-24.1—19.4)。
Full table
讨论
主要发现
本研究的目的是提供一个试验框架,以评估术前PVB对接受CCG正颌手术的患者术后阿片类药物用量的影响。同时还对疼痛评分和LOS进行了评估。就所有测量结果而言,接受术前PVB的组别与术前未接受PVB的组别之间没有统计学上的显著差异。本研究最显著的成果是为扩大这一主题的未来研究建立了框架,并确定了需要改进的领域,以更好地评估PVB的潜在益处。
优势和局限性
本研究具有明显的优势,对丰富OMFS研究作出了积极的贡献,但同时因为研究的回顾性本质和初步设计,也存在一些值得讨论的局限性。
作为第一项评估在进行CCG、同时进行正颌手术之前使用PVB的研究,本研究为未来的研究提供了基础,并确定了许多需要改进的方面,这一点对于探索新观点至关重要。本研究也适用于与OMFS相似的其他外科领域,如整形外科和耳鼻喉科,这些领域同样在头颈部周围进行手术,也进行CCG。
尽管本研究为未来的研究提供了跳板,但也存在明显的局限性。其中,最明显的局限性之一是样本量小。在我们的机构中,进行正颌外科手术的同时进行CCG的情况并不常见,因此只排除了<16岁的患者,而将其他患者都纳入了研究。鉴于样本量较小,应将本研究视作指导未来研究工作的初步研究(例如,样本量估计的功效分析)。实施一项大规模的多中心前瞻性研究可以收集更多样本量(如n>50),这将有助于确定PVB是否具有缓解CCG疼痛的潜在益处或减少阿片类药物用量的作用。
本研究的另一个局限性是患者之间手术缺乏同质性。尽管所有患者都接受了CCG和正颌外科手术,但有部分患者接受了其他手术,如颏整形术、颏成形术和拔牙。每例患者接受的不同手术组合可能导致不同程度的炎症和术后疼痛。未来的前瞻性研究应尝试根据即将进行的手术类型来匹配患者,以减少可能影响患者术后疼痛评分、阿片类药物需求和潜在的LOS的混杂因素。
虽然本研究并未发现各组之间在手术时间方面有统计学上的显著差异,但这一点仍可作为未来研究的有用指标。此外,在评估单次PVB与有导管的PVB时,手术时间可能是更重要的因素,因为手术时间较长时,PVB效果无法维持到手术结束,从而导致患者术后较早产生对阿片类止痛药的需求。
另外,本次研究为回归性研究,将患者分配到PVB组时并没有严格的分配隐藏和随机化方案,可能会导致选择偏倚。在本次研究中,每天由分配到区域麻醉小组的麻醉医生酌情为患者进行PVB。为了弥补这一局限性,利用正常生理盐水和局部麻醉药进行PVB的随机、双盲方案可以使患者和操作者无从知晓正在进行的治疗(即真正的PVB或PVB安慰剂)。然而,区域麻醉常常要求患者在手术前通过相应皮节分布的各种疼痛刺激来确认镇痛效果,因此很难做到让患者对其接受的治疗完全不知情。
此外,可以通过指定固定的外科医生和麻醉医生,使外科团队和麻醉团队的技能水平实现标准化。同样,未来的研究应努力统一使用或不使用PVB给药导管的情境。例如,在PVB组6例患者中,有3例接受单次阻滞,另外3例接受术后放置导管并给药。鉴于0.5%布比卡因的单次阻滞平均持续时间为9.9小时[19],通过导管输液当然有可能将镇痛效果延长到10小时以上,这使得两个亚组之间的比较变得复杂。样本量更大时,亚组人群也将更多,统计学比较效果更佳,如单次PVB和单次PVB加放置导管。值得注意的是,通过PVB导管进行药物输注,产生的局部麻醉效果可以随着时间的推移而累积,导致麻醉药的全身循环,从而在面部和胸部产生镇痛效果。在未来的研究中评估连续PVB组时,这些全身效应需要引起注意。
同样值得强调的是,尽管获取的肋骨都是患者的第5和(或)第6肋骨,但每名患者的PVB穿刺位置却不尽相同(表3)。PVB解剖学穿刺位置的变化以及单次阻滞和连续进行PVB都可能影响PVB的成功。在设计一致和可比的治疗方案时,应重点考虑PVB穿刺位置和类型的标准化。
另一个问题是患者术后的治疗差异。大多数患者是从PACU转到病房,但有2例患者由于后勤问题,如病房床位不足,而在PACU停留一晚。在本研究中,部分患者延长了在PACU的时间,而在PACU中他们可以得到ICU级别的护理,同时会更常规地使用更强效的阿片类药物控制疼痛,因此他们与非PACU的病房患者在PACU停留时间和疼痛评分方面的差异变得难以比较。此外,术后仍保留气管插管的患者常常因为主观报告的疼痛以外的原因而被给予阿片类药物,如在加强呼吸机同步时。同样,患者可能因无法口述疼痛评分而被减少阿片类药物的用量,如其他镇静药物使他们无法说话。因此,招募足够数量的患者进入研究,以排除方案异常值或进行进一步的亚组分析,将有助于提升研究结果的一致性和有效性。
鉴于非PVB组有5例患者在术后48小时内出院(即术后41.3、44.2、45.1、44.8和43小时),而PVB组有2例患者在同期内出院(即44.5和47.6小时),因此随访偏差也是一个值得关注的问题。鉴于本研究样本量较小,因此并未将这些患者排除。如果所有患者都在术后48小时内全程留观,那么各组的MED和疼痛评分的中位数可能会有所不同。本研究只考察院内阿片类药物的用量情况,尽管大多数患者出院时都开具了口服阿片类药物的处方,未来的研究可以跟踪这些处方的使用情况,以指导围手术期阿片类药物的处方习惯。
数据缺失同样对本研究产生了一些影响。对于数据缺失的患者,由OMFS手术人员手动搜索记录在其他地方的相关数据,如病历文件中。例如,在评估PVB的成功率时,缺乏关于每次PVB的作用时间或麻醉针穿刺的确切深度和位置的明确记录,因此要手动搜索麻醉记录以获得这些信息。同样,每台手术使用的CPT代码也有较大差异,很多都是人工修改的。许多手术缺少每种操作的适当CPT代码,但最终根据对手术名称或描述的搜索确定了这些代码。未来的研究必须考虑用多种方法搜索EHR,以确定符合条件的病例,特别是这类病例在OMFS中相对罕见,而且病例代码常出现错误。
最后,本研究的普遍性有限。这些手术往往需要住院、耗费大量资源,因此经常被转到三级或四级转诊中心,如进行本研究的相关医院。因此,本研究的结果最适用于大体量的OMFS中心,这类中心往往有OMFS住院医师项目,也具有进行相关手术的资源和专业知识。
与类似研究的比较
据我们所知,本研究是第一项评估PVB在CCG正颌手术中的作用的研究。
目前已发表的研究中关于头颈部手术中CCG供区疼痛的研究较少,且均不属于OMFS领域,例如,一项整形和重建外科领域的研究发现,在获取分层厚度肋软骨移植物时应用PVB,术后疼痛减轻[20]。同样,一项耳鼻喉科的试验性研究描述了PVB在减少第一阶段先天性小耳畸形修复CCG疼痛中的作用。但这些手术都没有获取肋骨,而肋骨是重建TMJ的CCG正颌手术的一个必要组成部分。
本研究发现两组之间的MED需求没有差异,尽管其他研究发现在类似的胸壁手术中应用PVB可以减少阿片类药物的使用[21-23]。因此,对于OMFS领域的研究而言,可以在我们的研究方案基础上扩增更大的样本量,才能证明PVB在胸壁周围手术中的有益作用,这在其他外科专业研究中也有发现。
此外,本研究的LOS中位数约为3天,与文献中的1.2~8.5天的范围相当[24]。这些研究结果表明,在进行CCG手术时,使用PVB并不能改善LOS,这一发现曾在获取肋软骨进行小耳畸形修复的研究中描述过[23]。
最后,在本研究中,PVB没有已知的并发症,但其他研究报告了潜在的并发症,包括气胸、胸膜穿刺和血管穿刺[14,25]。鉴于存在气胸等并发症的风险,有观点主张只将PVB用于更具侵入性的胸壁手术(如乳房切除术),而避免将其用于小型手术,如乳房肿瘤切除术、乳房四分之一切除术、放射线定位乳房活检[25]。本研究作者认为,涉及骨和软骨切除的CCG是一种侵入性胸壁手术,根据上述标准,在这类手术中应用PVB是合理的。此外,对于6%~10%的患者,PVB可能无法提供足够的镇痛效果[14],这一比例与胸段硬膜外麻醉的失败率相当。然而,这一风险可能通过术前对阻滞进行充分测试或术中直接在CCG供区进行局部麻醉而得到改善。
对研究结果的解释
MED
我们假设,患者通过术前接受PVB可以降低术后在肋骨移植供区的疼痛,因此需要的阿片类药物用量也会减少。然而,本研究的结果未能发现PVB组和非PVB组在PACU/ICU、术后24小时和术后48小时的平均MED有统计学上的显著差异(表4)。在本研究的实施过程中存在很多障碍,从而影响了研究结果的统计学意义。首先,每组有一例患者术后保留气管插管直至术后第1天,使他无法在术后早期参与疼痛评分以指导麻醉药的使用。其次,由于插管患者使用的镇静药物具有一定的镇痛作用,以及为了避免呼吸机人机对抗需要应用麻醉药物,因此,这2例患者可能误导性地提高(或降低)了各组的MED需求,尽管这种潜在的偏倚在研究组之间得到了平衡。此外,每组中都有1例患者在术后第二天回病房前,滞留在PACU一晚。尽管PACU和病房的护士使用相同的NRS来评估疼痛,但PACU的患者群体与病房的手术和非手术患者群体不同,这可能会影响护理人员的观念和选择各种镇痛药的阈值。通过招募更大的样本量,未来的前瞻性研究有可能减轻这类异常患者的影响。
在评估阿片类药物的使用时,也可以考虑非阿片类药物的镇痛效果。目前已有公开的阿片类药物的换算系数[15-18],但对于非阿片类镇痛药,如酮咯酸三甲胺、布洛芬、对乙酰氨基酚、加巴喷丁或氯胺酮,却没有这种换算系数。因此,本研究无法控制或比较各组之间的非阿片类镇痛药的使用,也无法权衡它们对术后疼痛控制的影响。然而,由于我们机构将对乙酰氨基酚作为一线镇痛药物,在临床上对大多数术后患者常规使用,因此大多数本来需要阿片类药物的患者可能在使用麻醉药之前(或之外)就使用了对乙酰氨基酚。未来的研究最好能严格非阿片类镇痛药的使用规范,从而突出患者对阿片类药物的特殊需求。
疼痛评分
本研究还评估了术后在PACU/ICU、术后24小时和术后48小时的疼痛评分。我们假设PVB组的疼痛控制可能会得到改善,患者报告的疼痛评分也会因此降低。经研究发现,与非PVB组相比,PVB组在所有时间点的疼痛评分都较低,但组间没有统计学上的显著差异。一项混杂因素是疼痛评估没有记录疼痛的位置。同时涉及CCG的正颌手术中有两个手术部位(即胸部和面部),两个部位都可能出现疼痛。接受PVB的患者在获取肋骨部位的疼痛与面部疼痛相比可能更轻,也可能更重,但由于只记录了一个疼痛评分,因此无法区分主要的疼痛来源。
另外,能够报告疼痛评分是数据收集的一个必要条件。本研究中有1例非PVB组的患者和1例PVB组的患者直到术后第1天仍在插管,因此他们在术后早期无法报告疼痛评分。鉴于研究样本量较小,这些患者最终也被纳入研究,但如果未来的研究有更大的样本量,可能会允许排除这些患者,从而创造更多的可比性治疗方案。同样,也没有方案规定护理人员何时或多长时间评估一次NRS,这一点在未来的研究中需要加以注意。此外,鉴于个体之间疼痛体验的主观性和差异性,在未来的前瞻性研究中,通过血压计测试等方法在手术前校准参与者对疼痛的反应或敏感性将是有益的[26],血压计测试包括记录个人对紧缩血压袖带的疼痛反应。
LOS
文献记载,正颌外科患者的平均LOS为28.8~204小时[24,27],略低于本研究中报告的77~78小时的中位数。在我们的机构中,当患者能够自行排泄(即排尿),能够走到洗手间或在地板上走动,能够忍受超过约200 mL的口服液摄入,并且疼痛能够通过口服方案得到控制而不需要静脉注射药物时,就符合出院标准。在未来的研究中考虑所有阻碍出院的因素可能有助于厘清疼痛对出院时间的影响,以及PVB对缩短出院时间的任何潜在影响。
可能的结果和需要采取的行动
尽管本研究受限于规模和统计学意义,不能得出PVB在CCG正颌手术中的作用的最佳评价结果,但却为未来的研究提供了一些有用的建议,我们将其列举如下。
- 通过延长研究入组时间、与其他机构合作和/或使用多种方法搜索EHR来确定符合条件的病例,特别是那些另类标记或非传统CPT代码的病例,使样本量最大化。患者量增加会使排除异常值或进行亚组分析更加可行。
- 分别评估面部和胸部的疼痛评分,以单独确定CCG供区疼痛。通过进行超声引导下的三叉神经阻滞最大程度地减轻面部疼痛[28],可以明确胸壁疼痛的程度。
- 尽量使用单一的疼痛评估评分系统,并为护理人员评估患者疼痛评分的频率确定方案。
- 为每例患者测定疼痛敏感性基线,如通过血压计测试[26],参考该基线将患者匹配到对照组和实验组。
- 还应根据患者面部手术的确切位置、手术次数、手术时间和PVB类型(单次注射与留置导管给药)来匹配患者。
- 考虑评估出院的具体障碍,以更好地了解它们对LOS的影响,包括与未接受PVB的患者相比,PVB是否能提供更好的疼痛控制从而缩短LOS。
- 考虑评估出院后的阿片类药物用量,以评估PVB对疼痛控制和阿片类药物需求的短期和长期影响。
- 考虑进行前瞻性研究,如随机、双盲方案(用生理盐水与局部麻醉药),以使患者和操作者对正在进行的治疗(即真正的PVB或PVB安慰剂)一无所知。固定手术团队和麻醉团队,只由少数操作者执行所有操作,将有助于规范治疗团队的技术水平。标准化每例患者接受PVB的确切位置也将有帮助。
结论
综上所述,本研究为第一项评估PVB在CCG正颌手术中的作用的研究。本研究是结果为阴性的初步研究,表明在正颌手术前接受PVB治疗CCG供区疼痛的患者与未接受PVB治疗的患者之间,在MED、疼痛评分或LOS方面没有统计学上的显著差异。虽然存在各种局限性,但本研究为未来的研究奠定了基础,使其能更好地量化PVB的效果,提升接受CCG和正颌手术患者的舒适度。
Acknowledgments
Prior presentations: an ePoster based on a smaller sample population of the current study was presented at the Anesthesiology 2021 Annual Meeting (Emery A, Deng H, Yang Q, Mueller A, Houle T, and Wang J. Single-shot Paravertebral Blockade For Autogenous Costochondral Graft Site Pain In Maxillofacial Surgery. Posterior session presented at: Anesthesiology 2021 Annual Meeting; 2021 Oct 9-13; San Diego, CA, USA).
Funding: None.
Footnote
Provenance and Peer Review: This article was commissioned by the editorial office, Journal of Oral and Maxillofacial Anesthesia, for the series “Opioid-free Anesthesia and Opioid-sparing Anesthesia in OMF Surgery”. The article has undergone external peer review.
Reporting Checklist: The authors have completed the STROBE reporting checklist. Available at https://joma.amegroups.com/article/view/10.21037/joma-22-23/rc
Data Sharing Statement: Available at https://joma.amegroups.com/article/view/10.21037/joma-22-23/dss
Conflicts of Interest: All authors have completed the ICMJE uniform disclosure form (available at https://joma.amegroups.com/article/view/10.21037/joma-22-23/coif). The series “Opioid-free Anesthesia and Opioid-sparing Anesthesia in OMF Surgery” was commissioned by the editorial office without any funding or sponsorship. JW serves as the unpaid editorial board member of Journal of Oral and Maxillofacial Anesthesia from August 2021 to July 2023 and served as unpaid Guest Editor of the series. The authors have no other conflicts of interest to declare.
Ethical Statement: The authors are accountable for all aspects of the work in ensuring that questions related to the accuracy or integrity of any part of the work are appropriately investigated and resolved. The study was conducted in accordance with the Declaration of Helsinki (as revised in 2013). The study was approved by institutional board of Massachusetts General Hospital (No. #2020P002222) and individual consent for this retrospective analysis was waived.
Open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), which permits the non-commercial replication and distribution of the article with the strict proviso that no changes or edits are made and the original work is properly cited (including links to both the formal publication through the relevant DOI and the license). See: https://creativecommons.org/licenses/by-nc-nd/4.0/.
References
- Choi MG. Temporomandibular joint reconstruction with costochondral graft: case series study. J Korean Assoc Oral Maxillofac Surg 2021;47:128-34. [Crossref] [PubMed]
- Khadka A, Hu J. Autogenous grafts for condylar reconstruction in treatment of TMJ ankylosis: current concepts and considerations for the future. Int J Oral Maxillofac Surg 2012;41:94-102. [Crossref] [PubMed]
- Kelley BW, Haggerty CJ. Costochondral Graft. In: Atlas of Operative Oral and Maxillofacial Surgery. Hoboken, NJ, USA: John Wiley & Sons, Inc., 2015:495-8.
- Emery AR, Deng H, Yang Q, et al. Single-shot Paravertebral Blockade For Autogenous Costochondral Graft Site Pain in Maxillofacial Surgery. Anesthesiology 2021. Annual Meeting: San Diego, CA, USA: 2021 Oct 9-13.
- James DR, Irvine GH. Autogenous rib grafts in maxillofacial surgery. J Maxillofac Surg 1983;11:201-3. [Crossref] [PubMed]
- Sharma H, Chowdhury S, Navaneetham A, et al. Costochondral Graft as Interpositional material for TMJ Ankylosis in Children: A Clinical Study. J Maxillofac Oral Surg 2015;14:565-72. [Crossref] [PubMed]
- Uppal RS, Sabbagh W, Chana J, et al. Donor-site morbidity after autologous costal cartilage harvest in ear reconstruction and approaches to reducing donor-site contour deformity. Plast Reconstr Surg 2008;121:1949-55. [Crossref] [PubMed]
- Sharma R, Louie A, Thai CP, et al. Chest Wall Nerve Blocks for Cardiothoracic, Breast Surgery, and Rib-Related Pain. Curr Pain Headache Rep 2022;26:43-56. [Crossref] [PubMed]
- D'Ercole F, Arora H, Kumar PA. Paravertebral Block for Thoracic Surgery. J Cardiothorac Vasc Anesth 2018;32:915-27. [Crossref] [PubMed]
- Huan S, Deng Y, Wang J, et al. Efficacy and safety of paravertebral block versus intercostal nerve block in thoracic surgery and breast surgery: A systematic review and meta-analysis. PLoS One 2020;15:e0237363. [Crossref] [PubMed]
- Wu C, Ma W, Cen Q, et al. A comparison of the incidence of supraventricular arrhythmias between thoracic paravertebral and intercostal nerve blocks in patients undergoing thoracoscopic surgery: A randomised trial. Eur J Anaesthesiol 2018;35:792-8. [Crossref] [PubMed]
- Hutchins J, Sanchez J, Andrade R, et al. Ultrasound-Guided Paravertebral Catheter Versus Intercostal Blocks for Postoperative Pain Control in Video-Assisted Thoracoscopic Surgery: A Prospective Randomized Trial. J Cardiothorac Vasc Anesth 2017;31:458-63. [Crossref] [PubMed]
- Ouerghi S, Frikha N, Mestiri T, et al. A prospective, randomised comparison of continuous paravertebral block and continuous intercostal nerve block for post-thoracotomy pain. Southern African Journal of Anaesthesia and Analgesia. 2008;14:19-23. [Crossref]
- Piraccini E, Pretto EA Jr, Corso RM, et al. Analgesia for thoracic surgery: the role of paravertebral block. HSR Proc Intensive Care Cardiovasc Anesth 2011;3:157-60. [PubMed]
- Leung JM, Sands LP, Chen N, et al. Perioperative Gabapentin Does Not Reduce Postoperative Delirium in Older Surgical Patients: A Randomized Clinical Trial. Anesthesiology 2017;127:633-44. [Crossref] [PubMed]
- Reddy A, Vidal M, Stephen S, et al. The Conversion Ratio From Intravenous Hydromorphone to Oral Opioids in Cancer Patients. J Pain Symptom Manage 2017;54:280-8. [Crossref] [PubMed]
- Rauck RL, Bookbinder SA, Bunker TR, et al. A randomized, open-label study of once-a-day AVINZA (morphine sulfate extended-release capsules) versus twice-a-day OxyContin (oxycodone hydrochloride controlled-release tablets) for chronic low back pain: the extension phase of the ACTION trial. J Opioid Manag 2006;2:325-8, 331-3. [Crossref] [PubMed]
- Mercadante S, Ferrera P, Villari P, et al. Frequency, indications, outcomes, and predictive factors of opioid switching in an acute palliative care unit. J Pain Symptom Manage 2009;37:632-41. [Crossref] [PubMed]
- Karmakar MK. Thoracic paravertebral block. Anesthesiology 2001;95:771-80. [Crossref] [PubMed]
- Gaba S, Gupta R, Mishra B, et al. Harvesting split thickness costal cartilage graft. Indian J Plast Surg 2017;50:79-81. [Crossref] [PubMed]
- Wang L, Wang Y, Zhang X, et al. Serratus anterior plane block or thoracic paravertebral block for postoperative pain treatment after uniportal video-assisted thoracoscopic surgery: a retrospective propensity-matched study. J Pain Res 2019;12:2231-8. [Crossref] [PubMed]
- Rivedal DD, Nayar HS, Israel JS, et al. Paravertebral block associated with decreased opioid use and less nausea and vomiting after reduction mammaplasty. J Surg Res 2018;228:307-13. [Crossref] [PubMed]
- Shaffer AD, Jabbour N, Visoiu M, et al. Paravertebral Nerve Block for Donor Site Pain in Stage I Microtia Reconstruction: A Pilot Study. Otolaryngol Head Neck Surg 2016;154:898-901. [Crossref] [PubMed]
- Bowe CM, Gurney B, Sloane J, et al. Operative time, length of stay and reoperation rates for orthognathic surgery. Br J Oral Maxillofac Surg 2021;59:163-7. [Crossref] [PubMed]
- Terheggen MA, Wille F, Borel Rinkes IH, et al. Paravertebral blockade for minor breast surgery. Anesth Analg 2002;94:355-9. table of contents. [Crossref] [PubMed]
- Butler S, Draleau K, Heinrich R, et al. Evaluation of Using the Sphygmomanometer Test to Assess Pain Sensitivity in Chronic Pain Patients vs Normal Controls. Pain Med 2020;21:2903-12. [Crossref] [PubMed]
- Chang FS, Burrows SA, Gebauer DP. Patient-Controlled Analgesia and Length of Hospital Stay in Orthognathic Surgery: A Randomized Controlled Trial. J Oral Maxillofac Surg 2019;77:818-27. [Crossref] [PubMed]
- Kumar A, Sinha C, Kumar A, et al. Ultrasound-guided trigeminal nerve block and its comparison with conventional analgesics in patients undergoing faciomaxillary surgery: Randomised control trial. Indian J Anaesth 2018;62:871-5. [Crossref] [PubMed]

夏明
上海交通大学医学院附属第九人民医院麻醉科副主任医师,副教授,硕士研究生导师,人工智能课题组长。Journal of Medical Artificial Inteligence(JMAI)主编,Journal of Oral and Maxillofacial Anesthesia(JOMA)执行主编,中华口腔医学会口腔麻醉专业委员会全国常务委员,中华口腔医学会镇静镇痛专委会全国常务委员,中国康复学会疼痛康复专委会全国委员。(更新时间:2023-01-16)
(本译文仅供学术交流,实际内容请以英文原文为准。)
Cite this article as: Emery AR, Deng H, Yang Q, Mueller A, Houle T, Wang J. The effects of paravertebral nerve blockade on post-operative pain for patients undergoing simultaneous autologous rib grafting and orthognathic surgery: a retrospective pilot study. J Oral Maxillofac Anesth 2022;1:32.




